В таблице Менделеева более сотни элементов, которые могут связываться друг с другом. Однако даже соединения, состоящие из одного химического элемента могут быть разнообразны.
Аллотропией называют явление существования одного химического элемента в виде двух или более простых веществ. Его открывателем по праву считается химик и минеролог из Швеции Йенс Берцелиус.
Аллотропия – это явление, которое имеет много общего с полиморфизмом кристаллов. Это вызвало долгие споры среди ученых. В настоящее время они пришли к мнению, что полиморфизм характерен только для твердых простых веществ.
Каждый химический элемент в таблице Менделеева — это определенный вид атомов со своими уникальными свойствами. Однако в природе существует не так много веществ, которые состоят из скоплений атомов. Кислород, углекислый газ, вода и множество других соединений представляют собой молекулы.
Атом кислорода и молекула кислорода сильно отличаются друг от друга по своим свойствам. Так или иначе, в природе атомы кислорода склонны объединяться и образовывать молекулы, потому что это энергетически более выгодно. Но один химический элемент может образовывать сразу несколько видов молекул. Например, если соединить два атома кислорода, можно получить молекулу O2, а если соединить три атома, то получится уже озон O3.
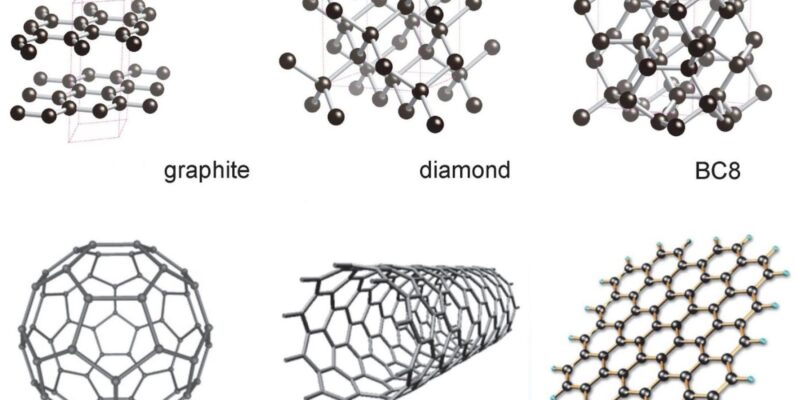
Явление образования множества химических веществ из одного химического элемента называется аллотропией, а эти вещества — аллотропными модификациями. Самый известный пример, иллюстрирующий это явление — углерод. Этот элемент может принимать форму не только «беспорядочного» угля и уложенного в слои графита, но и графена, нанотрубок и фуллеренов, похожих на футбольные мячи.
Аллотропия позволяет сильно увеличить количество доступных человеку соединений. Многие модификации углерода сегодня используются в исследованиях для создания сенсоров, средств адресной доставки лекарств, а также упрочнения существующих конструкционных материалов.
Какие существуют аллотропные модификации углерода?
Графит
Этот минерал отлично знаком всем детям и взрослым, которые хоть раз держали в руках карандаш. Графит оставляет след, пачкает руки, если его потрогать, и имеет серо-черную окраску. Кроме того, эта аллотропная модификация углерода хорошо проводит электричество и тепло, обладает жирной текстурой, которая позволяет графиту не растворяться в воде, и теплоустойчивостью. В промышленности его чаще всего используют для создания электродов, тиглей, огнестойких сосудов, огнеупорного кирпича, антикоррозионных красок и полировальных средств. Производят графит в основном в Китае, а в природе он встречает в графитовых или кристаллических сланцах.
Сера
Причина модификаций серы также заключается в особенностях внутренней структуры молекул. Самой устойчивой формой является ромбическая. Кристаллы этого вида аллотропии серы называют ромбоидальными. Каждый из них образован коронообразными молекулами, в состав каждой из которой входит 8 атомов. По физическим свойствам ромбическая сера является твердым веществом желтого цвета. Она не только не растворяется в воде, но даже не смачивается ею. Показатели тепло- и электропроводности очень низкие.
Структура моноклинной серы представлена параллелепипедом со скошенными углами. Визуально это вещество напоминает иглы темно-желтого цвета. Если серу расплавить, а потом поместить в холодную воду, образуется ее новая модификация. Ее первоначальная структура разрушится до полимерных цепей разной длины. Так получают пластическую серу – резиноподобную массу коричневого цвета.
Алмаз
Известный драгоценный камень, который по совместительству является аллотропной модификацией углерода. Среди всех минералов алмаз – самый твердый и при этом очень хрупкий. Выглядит он как кристалл с восемью или шестью гранями. В отличие от предыдущей модификации, алмаз совсем не проводит электричество, однако хорошо справляется с такой задачей для тепла. Добывают алмазы чаще всего в первичных кимберлитовых и россыпных месторождениях – такие обычно образовываются вследствие переноса. Многие знают, что после обработки алмазы становятся бриллиантами, однако этого достигают только высококачественные камни. Варианты низкого качества или синтетические кристаллы используются в качестве промышленного сырья. Например, из них делают лезвия, сверла и абразивы, медицинское и научное оборудование.
Фосфор
Ученые насчитывают 11 видов фосфора. Его аллотропия была открыта практически случайно, как и само это вещество. В поисках философского камня алхимик Бранд получил светящуюся сухую субстанцию в результате выпаривания мочи. Это был белый фосфор. Данное вещество характеризуется большой химической активностью. Достаточно повышения температуры до 40 градусов, чтобы белый фосфор вступил в реакцию с кислородом и воспламенился.
Для фосфора причина аллотропии – это изменение в структуре кристаллической решетки. Изменить ее можно только при определенных условиях. Так, увеличив давление и температуру в атмосфере углекислого газа, получают красный фосфор. Химически он менее активен, поэтому для него не характерно свечение. При нагревании он превращается в пар. Мы наблюдаем это каждый раз, зажигая обычные спички. Терочная поверхность как раз содержит красный фосфор.
Фуллерены
Фуллерены ученые открыли совсем недавно. Встречаются в природе они гораздо реже, чем те аллотропные модификации углерода, о которых мы рассказали до этого. На вид фуллерены – коричневые или черные полупрозрачные твердые вещества, обладающие металлическим блеском. По структуре и форме они могут быть разными: более и менее прочными, многослойными или цилиндрическими. Их молекулы не могут растворяться в воде и не имеют химической активности, обладают полупроводниковыми и сверхпроводящими свойствами. Добывают фуллерены их сажи, а используют в электронной, оптической, биомедицинской и нанотехнологической промышленности.
Графен
Еще одна аллотропная модификация углерода, о которой наука узнала не так давно. На вид графен – плоская структура из отдельных атомов углерода, которые располагаются по принципу сот. Толщина графена – всего один атом, при этом он очень твердый и устойчивый к растяжению. Материал хорошо проводит как тепло, так и электричество, обладает прозрачностью и очень большой скоростью потока электронов. В промышленности его используют для производства быстродействующих транзисторов, спиральных сенсорных дисплеев или фотоэлектрических модулей с батареями для хранения энергии. Часто графен добывают с помощью осаждения из газовой фазы и термического разложения карбида кремния.
Модификации железа
В качестве примера можно привести γ-железо, α-железо, δ-железо. У каждого из них отличные от других свойства, а также область применения, например, α-железо востребовано для производства стали, а γ-железо – для выпуска магнитов.
Циклоуглерод
Наконец, самая «юная» аллотропная модификация углерода – циклоуглерод. На вид это кольцо из 18 атомов углерода, между которыми чередуются одинарные и тройные связи. Ученые пока что не установили точные свойства циклоуглерода, но некоторые исследования показали, что он является полупроводником. Предполагается, что в будущем эту модификацию смогут использовать для миниатюризации электронных устройств.
Итак, аллотропия – это существование одного химического элемента в виде нескольких простых веществ. Чаще всего встречается среди неметаллов. Основными причинами этого явления считаются разное количество атомов, образующих молекулу вещества, а также изменение конфигурации кристаллической решетки.
Понравилась статья? Поделитесь с друзьями!
Без активной гиперссылки на материал Sauap.org копирование запрещено!
Ссылки: https://www.techinsider.ru/editorial/619123-chto-takoe-allotropiya-i-pochemu-ona-vazhna/, https://fb.ru/article/351131/allotropiya—eto-opredelenie-ponyatiya-i-prichinyi?ysclid=lj5fpe1njm815211293