фото: https://fb.ru/media/i/2/1/7/6/4/4/i/217644.jpg
В ходе исследований на мышах исследователи обнаружили доказательства того, что здоровый баланс кишечных микроорганизмов важен для хорошего здоровья. Рассказывает Sauap.org со ссылкой на Impulsa.
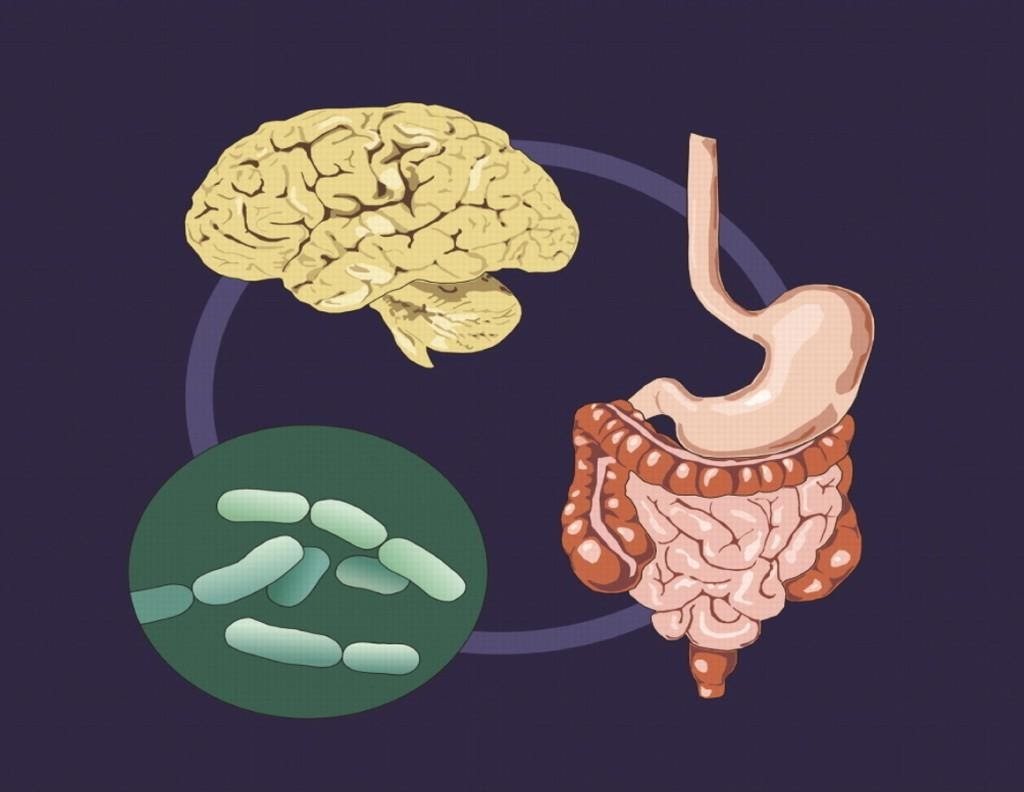
Исследователи из Института Пастера, Французского национального центра научных исследований (CNRS) и Inserm обнаружили доказательства того, что микробиота кишечника также играет роль в регуляции настроения и работе мозга.
Микробиота кишечника — это сообщество бактерий, грибов и вирусов, обитающих в пищеварительном тракте.
Полученные данные исследований на мышах позволяют предположить, что изменения кишечных бактериальных сообществ могут привести к депрессии или способствовать ей. Если у людей есть аналогичный механизм, врачи могли бы использовать штаммы бактерий для лечения расстройств настроения, таких как депрессия.
Исследование, проведенное группой из 16 исследователей из нескольких известных французских исследовательских институтов провела исследование, было опубликовано в Nature Communications.
Микробиота кишечника и настроение
Исследования показали, что некоторые люди, страдающие депрессией, страдают дисбактериозом, который представляет собой дисбаланс или изменение микробиоты кишечника.

фото: https://sektascience.com/
Исследования, проведенные на грызунах, также показывают, что дисбактериоз кишечника связан с неврологическими изменениями, связанными с депрессией, такими как:
- снижение нейрогенеза у взрослых, или роста новых клеток мозга;
- хроническое воспаление малой степени;
- ненормальная функция оси гипоталамус-гипофиз-надпочечники (HPA) (центральная система реакции организма на стресс).
Исследования на животных также показывают, что микробиота кишечника помогает регулировать беспокойство. Она также может влиять на развитие неврологических состояний, вызванных дисфункцией контуров, таких как болезнь Паркинсона, болезнь Альцгеймера, депрессия и обсессивно-компульсивное расстройство.
Исследователи считают, что это связано с тем, что кишечные бактерии выделяют метаболиты — крошечные кусочки пищи, расщепляемые при пищеварении, которые влияют на работу мозга. Метаболиты могут влиять на регуляцию настроения, воздействуя на эндоканнабиноидную систему.
Эндоканнабиноидная система — это сложная клеточная сигнальная система, состоящая из нейротрансмиттеров на основе липидов (жиров) и их рецепторов.
Она расположена по всему телу и играет роль в важных аспектах здоровья, таких как функции иммунной и нервной систем и клеточная связь в нервной системе. Она также регулирует эмоции, настроение и реакции на стресс за счет активации главного рецептора системы, CB1.
Предыдущие исследования подтверждают идею о том, что восстановление микробного здоровья кишечника может помочь в лечении депрессии. В исследованиях на животных пребиотики влияли на эмоциональное поведение. В исследованиях на людях добавление пребиотиков также улучшало настроение у людей с депрессией.
Но, несмотря на обоснованные теории, исследователи до сих пор не знают точно, как кишечные бактерии влияют на работу мозга.
Исследователи в недавнем исследовании намеревались найти механизмы, связывающие микробиоту кишечника и расстройства настроения. Группа исследователей из тех же французских институтов опубликовала в начале этого года отчет, в котором обнаружено, что вызванные стрессом изменения в микробиоте кишечника снижают эффективность антидепрессанта флуоксетина у мышей.
Исследование и его результаты
В ходе исследования исследователи подвергали генетически идентичных мышей воздействию непредсказуемого хронического легкого стресса (UCMS), модели стресс-индуцированной депрессии на мышах, в течение 8 недель.
Это лечение привело к развитию у мышей депрессивно-подобного поведения, такого как уменьшение количества еды, ухода за шерстью, потеря веса и нейрогенеза гиппокампа. Гиппокамп отвечает за обучение и память и сильно зависит от ряда психических и неврологических состояний.
Затем исследователи трансплантировали образцы фекалий, содержащие микробиоту кишечника, от контрольных мышей и мышей, подвергшихся воздействию UCMS, здоровым мышам. Чтобы служить контролем, мыши, которым была проведена трансплантация фекалий, были лишены микробов кишечника или получали лечение антибиотиками в течение 6 дней.
Через 8 недель у мышей, получивших трансплантаты от мышей UCMS, развились симптомы депрессии. У мышей также наблюдалось уменьшение количества новых стволовых клеток мозга и нейронов в гиппокампе.
Эти результаты показывают, что перенос кишечной микробиоты от депрессивных мышей со стрессом к здоровым мышам вызывает подобное депрессивному поведение.
«Удивительно, но простой передачи микробиоты от животного с расстройствами настроения животному с хорошим здоровьем было достаточно, чтобы вызвать биохимические изменения и вызвать у последнего депрессивное поведение», – отмечает Пьер-Мари Льедо, руководитель отдела восприятия и памяти в Институте Пастера (CNRS / Institut Pasteur), один из авторов исследования.
Чтобы выяснить, как это произошло, исследователи изучили возможность того, что микробиота, подвергшаяся воздействию UCMS, может вызывать депрессию, изменяя метаболизм. Они обнаружили, что у мышей с микробиотой UCMS значительно снизился уровень определенных жирных кислот в крови и мозге.
Восстановленные жирные кислоты включают моноацилглицерины (МАГ), диацилглицерины (ДАГ), полиненасыщенные жирные кислоты и линолевую кислоту. Варианты двух из этих жирных кислот превращаются в эндоканнабиноиды (eCB).
Исследователи предполагают, что дисбактериоз кишечника может вызвать эти изменения в уровне жирных кислот. Исследования связывают нарушение регуляции эндоканнабиноидной системы и ее центрального рецептора CB1 с депрессией как у мышей с моделью UCMS, так и у людей.
В ходе исследования исследователи обнаружили, что у мышей с микробиотой UCMS значительно снизились уровни eCB в гиппокампе и крови. Они также обнаружили, что у мышей с микробиотой UCMS были снижены уровни бактерий Lactobacillus.
Исследователи смогли уменьшить депрессивное воздействие микробиоты UCMS за счет повышения уровня CB1 и перорального введения мышам штамма бактерий Lactobacillus.
Эти результаты показывают, что хронический стресс, диета и микробиота кишечника способствуют развитию депрессивно-подобного поведения через эндоканнабиноидную систему.
«Это открытие показывает роль кишечной микробиоты в нормальном функционировании мозга», – говорит Жерар Эберл, руководитель отдела микросреды и иммунитета (Institut Pasteur / Inserm) и автор исследования.
В частности, дисбаланс в кишечном бактериальном сообществе, снижающий уровень жирных кислот, жизненно важных для эндоканнабиноидной системы и функции мозга, по-видимому, способствует развитию депрессивно-подобного поведения.
Эти данные означают, что определенные бактерии могут действовать как естественный антидепрессант, лечить расстройства настроения путем восстановления микробного здоровья кишечника. И это многообещающие новости, учитывая множество потенциальных побочных эффектов и относительно низкую эффективность большинства современных антидепрессантов.
Чтобы подтвердить свои результаты, исследователям необходимо проверить свои выводы на людях. Исследователи говорят, что новое исследование также должно будет изучить, влияют ли изменения кишечной микробиоты на другие мишени эндоканнабиноидной системы мозга таким же образом.
Понравилась статья? Поделитесь с друзьями!
Без активной гиперссылки на материал Sauap.org копирование запрещено!